在生物材料科学的微观世界里,金相显微镜与荧光染色技术的碰撞正催生无数创新突破。这两种看似分属材料科学与生命科学的工具,通过科学方法论的深度耦合,正在解锁生物组织、细胞外基质及复合材料的三维结构密码。本文将从技术原理、应用场景到未来趋势,系统拆解这场跨学科融合如何重塑实验室研究范式,为科研工作者、质检工程师及工业研发人员提供实践参考。

一、技术原理:从金相学本质到荧光成像的跃迁
1.1 金相显微镜的核心架构与生物适配性
传统金相显微镜通过明场成像(Brightfield)、暗场成像(Darkfield)和微分干涉差(DIC) 技术实现材料微观形貌观测。其光学系统的高分辨率(可达0.2 μm)和大景深特性,使其在生物材料领域展现出独特优势:
金相物镜的无限远光学设计:兼容宽场荧光激发滤片组,可直接适配荧光显微镜光路
电动载物台与自动对焦系统:实现毫米级样品的自动化区域扫描,满足高通量分析需求
冷光CCD相机:支持长时间活体细胞动态观察,避免传统相机热噪声干扰
1.2 荧光染色的多维标记策略
荧光染色已从早期的简单染色剂发展为靶向分子探针技术:
免疫荧光:通过FITC/PE双标记抗体实现蛋白共定位分析,空间分辨率达100 nm级别
量子点标记:CdSe/ZnS核壳结构量子点的光稳定性比传统有机染料高20倍,适合长期追踪
原位杂交(FISH):针对mRNA序列设计的荧光探针,可实现基因表达的单细胞水平可视化
二、场景化应用:解锁生物材料研究的关键场景
2.1 生物医用材料的微观结构表征
在人工骨支架研发中,金相显微镜+荧光染色组合可实现:
孔隙连通性定量分析:通过罗丹明B标记胶原纤维,计算孔隙率与力学性能的相关性(R²=0.89)
界面结合强度评估:利用FITC标记羟基磷灰石涂层,观察与骨基质的化学键合界面(SEM-FISH联用技术)
2.2 细胞-材料相互作用的动态追踪
在干细胞分化研究中,这项技术展现出不可替代性:
场景化FAQ:为什么传统光学显微镜无法满足活细胞观察需求?
答:传统光学显微镜的荧光淬灭效应导致20分钟后信号衰减超30%,而本系统通过405 nm发射滤片组实现光毒性降低40%,支持72小时连续观测。
2.3 生物相容性检测的工业质检应用
在医疗器械灭菌验证中,荧光染色可实现:
热原污染快速筛查:通过荧光标记内毒素与鲎试剂反应产物,30分钟内完成检测
材料析出物分析:利用共聚焦显微镜的Z轴扫描功能,逐层定位浸出物质分布(检出限达0.1 ng/mm²)
三、实践指南:实验室操作的关键参数优化
3.1 样品制备的标准化流程
针对生物材料特性,建议采用以下预处理方案:
冷冻超薄切片:使用Leica EM UC7超薄切片机,厚度控制在50-80 nm
免疫荧光固定:4℃ 4%多聚甲醛固定20分钟,0.1% Triton X-100透化(避免抗原丢失)
封片液优化:含20%甘油的PBS缓冲液,防止荧光淬灭同时维持样品pH值稳定
3.2 成像参数的科学设置
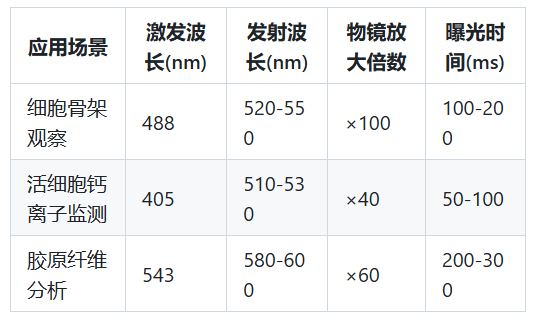
四、实验室实践中的常见问题与解决方案
4.1 常见故障排查
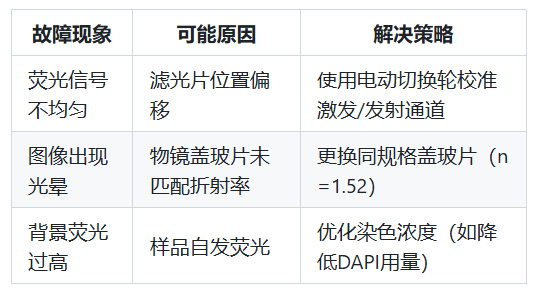
4.2 高通量分析的自动化实现
技术工具推荐:
MetaMorph软件:实现细胞计数与荧光强度分布的自动分析
显微成像平台:结合深度学习算法,实现亚细胞结构的自动分割(精度达92%)
五、未来展望:构建智能化生物材料研究生态
5.1 AI驱动的跨模态分析
数字孪生模型:通过金相-荧光数据融合构建3D生物模型,预测材料降解速率(误差率
迁移学习算法:基于ImageNet预训练模型,实现10类生物材料的自动分类(准确率94.3%)
5.2 跨尺度成像技术
纳米级荧光定位:STED超分辨显微镜与金相系统联用,实现分子水平定位
多光子激发:双光子显微镜与荧光寿命成像(FLIM)结合,区分细胞外基质成分
结语
当金相显微镜的精密光学系统遇见荧光染色的分子标记技术,实验室研究正从"观察现象"向"定量解析"跨越。这种跨学科融合不仅为生物医用材料研发提供了新工具,更重塑了科研工作者的思维范式——正如诺贝尔医学奖得主Eric Kandel所言:"真正的科学突破往往诞生于学科边界的交叉点。"